Hormonální regulace sacharidů a metabolismu lipidů
Video: Diabetes mellitus Program Ekdistan
Hlavními zdroji energie živých organismů - sacharidy a tuky mají vysoký prostor pro potenciální energie, snadno extrahuje z těchto buněk s použitím enzymu katabolické reakce. Energie uvolněná během biologických oxidačních produktů metabolismu sacharidů a tuků a glykolýzu se převede do velké míry na chemickou energii fosfátových vazeb ATP je syntetizován.Nahromaděné v chemické energie ATP-energetických vazeb, je zase strávil na různé typy buněk, práce - vytváření a udržování elektrochemických gradientů, svalové kontrakce, a některé sekreční transportních procesů, biosyntézy proteinů, mastných kyselin, atd Kromě „paliva“ funkcemi sacharidů a tuků spolu s proteiny slouží jako důležité nabízející budovy, plastových materiálů, obsažených v základní struktuře buněk - nukleových kyselin, jednoduché proteiny, glykoproteiny, lipidy, a tak na řadě
Syntetizovaný rozpadem sacharidů a ATP tukových buněk zajišťuje nejen potřebnou energii k práci, ale také je zdrojem cAMP, a je také zapojen do regulace aktivity mnoha enzymů, strukturních proteinů státu, zajistit jejich fosforylaci.
Sacharidů a lipidů substráty přímo recyklovatelných buňky jsou monosacharidy (hlavně glukózy) a neesterifikovaných mastných kyselin (NEFA) a v některých tkáních ketolátky. Jejich zdrojem jsou potraviny nasávána ze střeva, uložené v orgánech, ve formě glykogenu ve formě sacharidů a lipidů, neutrálních tuků, stejně jako non-sacharidy prekurzorů, zejména aminokyselin a glycerolu tvoří sacharidy (glukoneogeneze).
Ukládáním orgány u obratlovců zahrnují játra a tuk (tukové) tkáně, orgánů glukoneogeneze - játra a ledviny. Hmyz ukládání tělo je tuk tělo. Navíc zdroje glukózy a NEFA mohou být některé náhradní nebo jiné potraviny uložené nebo vytvořené v pracovní kleci. Různé způsoby a fáze metabolismu sacharidů a tuků jsou propojeny četnými vzájemnými vlivy. Směr a intenzita proudu těchto metabolických procesů závisí na řadě vnějších a vnitřních faktorů. Mezi ně patří zejména množství a kvalita potravin spotřebuje a jeho rytmy do organismu, úroveň svalové a nervové aktivity, atd
Tělo zvíře přizpůsobí povaze potravin režimu na nervové nebo svalové zátěže prostřednictvím komplexní sady koordinačních mechanismů. To znamená, že řízení toku různých reakcí v sacharidů a metabolismu lipidů provedena na koncentraci buněčné úrovni příslušných substrátů a enzymů, a stupeň nahromadění produktů konkrétní reakci. Tyto kontrolní mechanismy jsou mechanismy samoregulace a realizovány v jednobuněčných a mnohobuněčných organismů.
Posledně uvedené nařízení využití sacharidů a tuků se může objevit na úrovni interakce buňka-buňka. Zejména oba typy výměny vzájemně vzaimokontroliruyutsya: NEFA sval inhibuje odbourávání produktů glukózy jako zhroucení glukózy v tukové retard tvorbě NEFA. Ve většině vyšší zvířata dostávají na konkrétní mechanismus intracelulární regulace metabolismu meziproduktu určeného výskytu v evoluci endokrinního systému, který má rozhodující význam v kontrole metabolických procesů celého organismu.
Mezi hormonů podílejících se na regulaci lipidů a metabolismu sacharidů u obratlovců, centrální místo, je obsazena následujícími: hormony gastrointestinálního traktu, které ovládají trávení a vstřebávání produktů štěpení v krov- inzulínu a glukagonu - specifické regulátory meziprodukt metabolismus sacharidů a lipidov- STG a funkčně souvisejících s ním „somatomediny“ a CIF glkzhokortikoidy, ACTH a adrenalinu - nespecifické faktory adaptace. Je třeba poznamenat, že mnohé z výše jmenovaných hormonů také se přímo účastní na regulaci metabolismu proteinů (viz. Kap. 9). Míra sekrece hormonů a odkazoval se na realizaci jejich účinků na tkaniny jsou vzájemně propojeny.
Nemůžeme přebývat konkrétně na fungování hormonálních faktorů, gastrointestinálního traktu, je secernován do neuro-humorální fáze sekrece. Jejich hlavní účinky jsou dobře známy v průběhu všeobecných fizilogii lidí a zvířat a kromě toho z nich už dostatečně uvedeno v kap. 3. Více podrobně intersticiální regulace endokrinní metabolismu sacharidů a tuků.
Hormony a regulace intersticiální metabolismu glukózy. Integrační indikátor bilance metabolismu sacharidů v těle obratlovců je koncentrace glukózy v krvi. Tento údaj je stabilní při savčí asi 100 mg% (5 mmol / l). Jeho deformace obvykle zpravidla nepřesahuje ± 30%. Hladina glukózy v krvi, závisí na jedné straně tím, že přítok krve převážně monosacharidu od střev, jater a ledvin, a na druhé straně - na svém odtoku do pracovní a depotní tkání (Obrázek 95).

Obr. 95 způsoby, jak udržují dynamické rovnováhy glukózy v krvi
Membrány svalových buněk a adiloznyh mají "bariéru", k dopravě glyukozy- GL-6-f - glukóza-6-fosfát
Příliv glukózy z jater a ledvin je určen poměrem aktivní a glikogenfosforilaznoy glikogensintetaznoy reakce v játrech, je poměr intenzity zhroucení glukózy a glukoneogeneze v játrech intenzity a částečně v ledvinách. Příjem glukózy v krvi je v přímé korelaci s úrovněmi fosforylázy reakce a glukoneogeneze procesu.
Odtok glukózy z krve do tkání je přímo závislá na rychlosti jeho dopravy do svalů, tukových a lymfoidních buněk, membrány, které poskytují bariéru proti pronikání glukózy (připomeňme, že membrány jaterních buněk, mozku a ledvinách snadno propustný pro monosacharid) - metabolické využití glukózy, v závislé na propustnosti membrány k ní a činnost klíčových enzymů se rozpadá přeměnu glukózy do glykogenu v jaterních buňkách otáčky (Levin et al., 1955 Nyuskholm, Randle, Foa 1964- 1972).
Všechny tyto procesy jsou spojené s dopravou a metabolismu glukózy, přímo řízen komplexní hormonální faktory.
Hormonální regulátor metabolismu sacharidů působením celkového směru úrovní výměny a hladina glukózy v krvi je možno rozdělit do dvou typů. První typ hormon stimuluje využití tkáň glukózy a jeho ukládání ve formě glykogenu, ale inhibuje glukoneogenezi, a tudíž způsobuje snížení koncentrace glukózy v krvi.
Hormonální akce tohoto typu se inzulín. Druhý typ hormonů stimuluje odbourávání glykogenu a glukoneogenezi, a tudíž způsobuje zvýšení hladiny glukózy v krvi. Pro tento typ hormonů zahrnují glukagonu (a sekretin a VIP) a adrenalin. Hormony Třetí typ stimulují jaterní glukoneogeneze, inhibují využití glukózy od různých buněk a zároveň podpořit tvorbu glykogenu hepatocytů, což vede k převaze prvních dvou efektů tendenci také zvyšovat hladiny glukózy v krvi. Pro tento typ hormonů patří glukokortikoidy a růstový hormon - „somatomediny“. Avšak to, že jednosměrný vliv na procesy glukoneogeneze, syntéza glykogenu a glykolýzu, glukokortikoidy a růstový hormon - „somatomediny“ mají různé účinky na propustnost buněčných membrán svalů a tukové tkáně glukózy.
Orientací účinku na koncentraci glukózy v krvi je hypoglykemické hormon inzulín (hormon „klidový a nasycení“), hormony druhé a třetí typů - hyperglykemické (hormonů „a nalačno stresových“) (Obrázek 96).

Obrázek 96. Hormonální regulace homeostázy sacharidů:
pevné šipky označuje stimulační účinek přerušovaná - inhibice
Inzulín je hormon, může být nazýván asimilaci a ukládání sacharidů. Jedním z důvodů pro zvýšení využití glukózy ve tkáni je stimulace glykolýzy. To se provádí, případně na úrovni aktivace klíčových enzymů glykolýzy hexokinázou, zejména jeden z jejích čtyř známých izoforem - II hexokinase a glukokináza (Weber, 1966 a Ilyin, 1966, 1968). Zdá se, že roli při stimulaci katabolismus glukózy a inzulínu hraje zrychlení pentózofosfátové cesty v kroku glukóza-6-fosfatdegidrogenaznoy reakce (Leites, Laptev, 1967). Předpokládá se, že stimulace vychytávání glukózy v játrech na jídlo hyperglykémie ovlivněna inzulínu hraje důležitou roli hormonální indukci specifických jaterních enzymů glukokinázy selektivně fosforylovat glukózy při vysokých koncentracích.
Hlavním důvodem pro stimulaci využití glukózy svalových a tukových buněk - zejména selektivní zvýšení propustnosti buněčných membrán na monosacharid (Lunsgaard 1939 Levin, 1950). Tak je dosaženo zvýšením koncentrace substrátů pro hexokinas reakci a pentózofosfátové cesty.
Amplifikace glykolýza ovlivněn inzulínu v kosterním svalu a myokardu hraje významnou roli v akumulaci ATP a zajišťujících svalových buněk provozuschopnosti. Amplifikace jater Glykolýza zdá důležité nejen pro zvýšení zahrnutí pyruvátu v dýchání systému tkáně, jako pro akumulaci acetyl-CoA a malonyl-CoA jako tvorba prekurzor vícemocný mastných kyselin a následně triglyceridů (Nyuskholm, start, 1973) ,
Vytvořená během glykolýza glycerofosfát se také podílí na syntéze neutrálního tuku. Kromě toho, v játrech, a to zejména v tukové tkáni lipogeneze zlepšit glukóza hraje důležitou roli hormonální stimulaci glukózo-6-fosfatdegidrogenaznoy reakce vedoucí ke vzniku NADPH - snížení kofaktoru nezbytné pro biosyntézu mastných kyselin a glycerofosfát. Tak u savců nasáván pouze 3-5% glukózy převede na jaterní glykogen, spíše než 30% se akumuluje jako tuk uložen v depotních orgánech.
To znamená, že hlavní směr působení inzulínu na glykolýzy a pentozofoofatny dráhy v játrech a tukové tkáni, zejména je zajistit tvorbu triglyceridů. U savců a ptáků v tukových buněk, a v nižších obratlovců v hepatocytech glukózy - jedním z hlavních zdrojů uložení triglyceridů. V těchto případech je fyziologický význam hormonální stimulace využití uhlohydrátů je snížena do značné míry na stimulaci lipidového povlaku. Současně inzulínu má přímý vliv na syntézu glykogenu - vklad formě sacharidů - a to nejen v játrech, ale i ve svalu, ledvinách a případně tukové tkáně.
Hormon působí stimulační účinek na glikogenoobrazovanie, zvyšující aktivitu glykogenu (D-přechodu neaktivní formu na aktivní I-tvar) a inhibiční glykogenfosforylázy (6-přechod inaktivní formě v L-formě), a tím inhibuje glykogenolýzu v buňkách (obr. 97). Oba účinek inzulínu na těchto enzymů v játrech zprostředkované, se zdá, že je aktivace membránových proteinázy akumulačních glykopeptidů, aktivace cAMP fosfodiesterázy.

Obrázek 97. Hlavní fáze glykolýzy, glukoneogeneze a syntézy glykogenu (v Ilin, 1965 modifikovaná)
Další důležitou oblastí působení inzulínu na metabolismus sacharidů je inhibice glukoneogeneze v játrech (Krebs, Ilin 1964-, 1965- Ikston et al., 1971). Inhibice glukoneogeneze provádí na úrovni hormonů snížená syntéza klíčových enzymů a fosfoenolpiruvatkarboksikinazy fruktozo- 16 difosfatazy. Tyto účinky jsou zprostředkovány také zvyšuje rychlost tvorby glykopeptidů - mediátorů hormonu (Obrázek 98).
Glukóza ve všech fyziologických stavech - hlavním zdrojem zásobování nervových buněk. Se zvýšením sekrece inzulínu, je určité zvýšení vychytávání glukózy nervové tkáně, patrně stimulací to glykolýzy. Avšak při vysokých koncentracích hormonu v krvi, což způsobuje hypoglykemii, dochází cerebrální sacharidů hladovění, a inhibice jeho funkce.
Po podání velmi velkých dávek inhibice inzulinu hlubokých center mozku může vést k rozvoji záchvatů, poté k bezvědomí a snižovat krevní tlak. Tento stav nastane, když se koncentrace glukózy v krvi nižší než 45-50 mg% se dále označuje jako inzulínu (hypoglykemického) šoku. Konvulzivní šok, a odpověď na inzulín se používá pro inzulínových přípravků biologické standardizace (Smith, 1950 Stewart, 1960).
VB Rosen
Sdílet na sociálních sítích:
Podobné
 Protein pankreatitida
Protein pankreatitida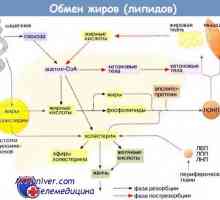 Tuku metabolismus v těle. Transport lipidů
Tuku metabolismus v těle. Transport lipidů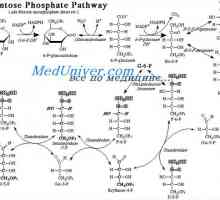 Uvolnění energie z glukózy přes pentózofosfátovém cyklu. Přeměna glukózy k tuku
Uvolnění energie z glukózy přes pentózofosfátovém cyklu. Přeměna glukózy k tuku Volné mastné kyseliny. Doprava volné mastné kyseliny
Volné mastné kyseliny. Doprava volné mastné kyseliny Tuk metabolismus a vylučování. játra tuk
Tuk metabolismus a vylučování. játra tuk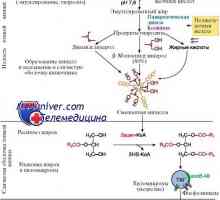 Vzdělávání v játrech acetoacetátu. Ketóza během půstu, a závislost na tučných jídel
Vzdělávání v játrech acetoacetátu. Ketóza během půstu, a závislost na tučných jídel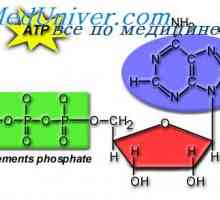 Uvolňování energie z potravin. Fyziologie adenosintrifosfátu (ATP)
Uvolňování energie z potravin. Fyziologie adenosintrifosfátu (ATP)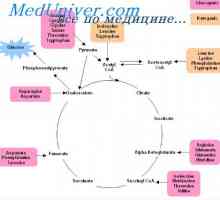 Syntéza triglyceridů z sacharidů. Stupních syntézy tuku z cukrů
Syntéza triglyceridů z sacharidů. Stupních syntézy tuku z cukrů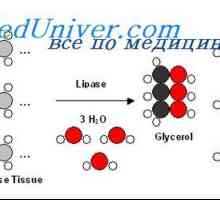 Triglyceridy syntéza proteinů. Regulace uvolňování energie triglyceridů
Triglyceridy syntéza proteinů. Regulace uvolňování energie triglyceridů Hormonální regulace metabolismu tuků. obezita
Hormonální regulace metabolismu tuků. obezita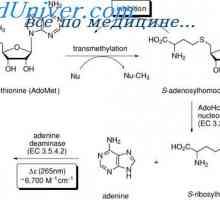 Rozdělení proteinů. Fyziologie členění regulace protein
Rozdělení proteinů. Fyziologie členění regulace protein Fyziologie výživy. dieta
Fyziologie výživy. dieta Játra makrofágů systém. Metabolické funkce jater
Játra makrofágů systém. Metabolické funkce jater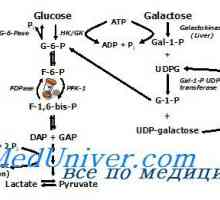 Kreatinfosfátu funkce. Anaerobní mechanismus energie
Kreatinfosfátu funkce. Anaerobní mechanismus energie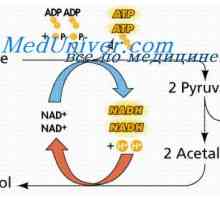 Využití v energetice buněk. Regulace uvolňování energie
Využití v energetice buněk. Regulace uvolňování energie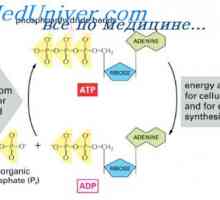 ADP roli při využívání energie. Intenzita metabolismu v buňkách
ADP roli při využívání energie. Intenzita metabolismu v buňkách Půst. Fyziologie vyčerpání při hladovění
Půst. Fyziologie vyčerpání při hladovění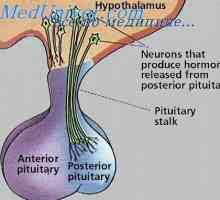 Úloha růstového hormonu v metabolismu tuků, Metabolismus sacharidů a růstový hormon
Úloha růstového hormonu v metabolismu tuků, Metabolismus sacharidů a růstový hormon Vliv hypofýzy v metabolismu tuků. Ateroskleróza při poruchách metabolismu sacharidů
Vliv hypofýzy v metabolismu tuků. Ateroskleróza při poruchách metabolismu sacharidů ATP a jeho role v buňce. Funkce buněčné mitochondrie
ATP a jeho role v buňce. Funkce buněčné mitochondrie Fyziologická význam hlavních složek potravy. Tuků a sacharidů
Fyziologická význam hlavních složek potravy. Tuků a sacharidů