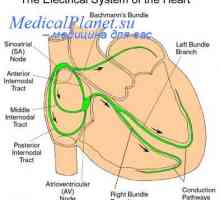
Porodnictví a ginekologiyarol buněčné faktory v progresi rakoviny děložního čípku
Rakovina děložního čípku je jednou z nejčastějších opuholeyu žen, každý rok tam je asi 500.000 nových sluchaevi více než 300.000 úmrtí. Nicméně, díky úspěchu dosáhl zaposlednie 15-20 let ve studiu etiologie a patogeneze tohoto onemocnění, tam byly skutečné přístupy ke snížení nemocnosti a úmrtnosti.Za prvé, je to kvůli vytvoření etiologických rolivirusov papilomy (HPV) ve výskytu rakoviny děložního čípku a vozmozhnostyusozdaniya specifických vakcín. Skupina virů papilloma vysokogoriska zahrnuje zejména HPV 16 a HPV 18 typy kotoryeassotsiirovany nejen k rakovině děložního čípku a jiných anogenitalnymiopuholyami, ale jsou také v 20% případů rakoviny nosoglotki.Nakopleno velkého množství důkazů o roliHPV v indukci rakoviny děložního čípku. Tato perzistence HPV DNA ve displaziyahi karcinomů tkáně, integrace a exprese virových genomav epiteliálních buněk, transformaci činnost virových onkogenovv pokusů in vitro.
Struktura a funkce produktů virových onkogenů E6 a E7 horoshoizucheny. Nejdůležitější je interakce s proteinem E6 r53s jeho následné degradaci. To má ten účinek analogichnoepo efektu somatické mutace p53: kontrolyaza průchod narušuje buněčného cyklu a jeho nežádoucí systému opravy DNA, která podporuje destabilizaci genomu. E6 také inhibuje apoptózu, produkci interferonu, buňka aktivuje telomerázy a kol. Klyuchevymdlya E7 je reakčním produktem tumor supresorového genu RBI uvolňování E2F transkripčního faktoru regulující kletochnuyuproliferatsiyu. Kromě toho, E7 vyvolává aktivaci cyklinu E a inaktivují inhibitory cyklin-dependentních kináz, podporuje a zvyšuje destabilizatsiihromosom mutagenní účinek chemického kantserogenov.Odnako, a to navzdory skutečnosti, že imortalizace účinnost povyshaetsyapri kooperativní účinek E6 a E7 exprese virového onkobelkovneobhodima ale nestačí pro imortalizaci normálních buněk následné malignit.
S tímto konzistentní důkazy z epidemiologických studií morfologicheskihnablyudeny. Dlouhá doba latence infekce prodolzhayuschiysyaobychno 10-20 let, skutečnost, že pouze malý počet infitsirovannyhzhenschin latentní infekci vede k rozvoji rakoviny, nádorů a monoklonální multifokalnostdisplazy obsahující integrirovannyevirusnye sekvencí ukazují, že infekce začíná virusompapillom vícestupňový proces, který znachitelnoystepeni řízena různými buněčnými faktory.
Zdá se, že významnou roli v regulaci funkce virové onkogenovi progrese mezi druhotné genetické izmeneniyam.Funktsionirovanie virové onkoproteiny způsobuje destabilizaci chromozómů, který může způsobit aktivaci onkogenů nebo inaktivace genů supressorov.Issledovanie role onkogenů v patogenezi rakoviny děložního čípku není vyyaviloprintsipialnyh změny v expresi většina z nich, pro isklyucheniemc-myc, a-fos a EGFR, a exprese EGFR v časném stadiyahukazyvaet špatnou prognózou.
Analýza specifických chromozomálních aberací pro lokalizaci vyyavleniyarayonov potenciální nádorové supresorové geny, inaktiviruemyhv v průběhu progrese nádoru prováděny cytogenetické techniky (FISH) nebo ztráta heterozygotnosti (LOH). AllelotipirovanieDNK ukázalo vysoké procento alelických ztrát na chromozomech 3,4, 5, 6, 11 a 18. Je zajímavé, že místo, na němž raspolagayutsyageny supresorových TP53 (17p) a RB (13p), není vysoce chastotoydeletsy. Na chromozomu 3, existuje více alelické ztráty loci 3r14.2, 3r21.3 a 3r24 3r25-26, kde 3r14.2 lokalizovangen FHIT, který je také odstraněna v nádorech ledvin, plic, prsu, ale není pravda, potlačující. Osobyyinteres představuje analýzu chromozomu 6p, který raspolagayutsyageny hlavního histokompatibilního komplexu: ztráta heterozygotnosti umístění genů oblast HLA třídy I a TNF (6r22-21.3) obnaruzhenav 50% nádorů. Nicméně, komplexní studie genotypu a třídy fenotipaHLA I ukázaly, že určité změny ve struktuře a narusheniyaekspressii mají až 90% nádorů. Tyto přestupky Zdá se, že hrají klíčovou roli ve schopnosti nádorových buněk izbezhatimmunnogo odpovědi.
Také jsme zjistili, časté alelické delece lokusu 6q16-21, které se předpokládá, že bude nacházet supresorový gen a gen indutsiruyuschiysenestsentsiyu. Význam některých genetických poruch mozhnootsenit korelace s klinickým stadiem nemoci. Narusheniyav loci 3r14.2 a 6r21.3 objeví na jevišti dysplazie, togdakak ztrátu heterozygotnosti na místech 6q16-21i 11q22-23 v korelaci ke vzniku metastáz. Proto existuje důvod se domnívat, že tyto lokusy jsou umístěny potenciální nádorové supresorové geny, které mají být identifikovány.
spolu s "regulace vnitřního signalizační kaskády"Důležitou roli v regulaci transkripce virového DNA prinadlezhittsitokinam. Je zjištěno, že kyselina retinová je effektivnopodavlyaet HPV přepis do imortalizovaných buněk podle comparisonwith maligní (imortalizace pravděpodobně sootvetstvuetklinicheskaya fáze mírné dysplazie). Stejný je sledován v otnosheniiregulyatsii retinová kyselina receptoru RAR b. Nicméně, interferon sochetaniis kyselina retinová se používá pro léčbu cervikální ploskokletochnogoraka. Interferony b a g jsou účinné v obou typech buněk, zatímco aktivita interferonu se liší v různých kulturahkletok. TGF-b účinně potlačuje transkripci virové imortalizace genovna kroku, ale ne v nádorech. Podobně deystviemobladayut TGF-a, interleukin-1 a leykoregulin. Jak se ukázalo, TGF-avliyaet složení transkripčního faktoru AP-1 předkladatele vzaimodeystvuyuschegos HPV. Imortalizované buňky, AP-1 se skládá s izgomodimera-jun / c-jun, a TGF-a léčba vede k posunu heterodimer s sobrazovaniem-jun / fra I a potlačení transkriptsiiHPV. Cuperekspressiya c-fos v imortalizovaných buněk s vyzyvaetobrazovanie heterodimeru-jun / c-fos a sootvetstvuyuschihklonov malignity.
To znamená, že úloha buněčných faktorů v různých stádiích HPV-indutsirovannogokantserogeneza se stává zřejmé.
Reference:
1. Kiselev FL Biochemistry, 65, 79 až 91 (2000).
2. Lazo PA., Br J Cancer, 80, 2008-2018 (1999).
3. zur Hausen H., J Nati Cancer Inst., 92, 690-698 (2000).
 Follow-up po léčbě cervikální dysplazie. Rakovina děložního čípku.
Follow-up po léčbě cervikální dysplazie. Rakovina děložního čípku. Aspirin a rakovina děložního čípku
Aspirin a rakovina děložního čípku Avastin prodlužuje životnost děložního hrdla stádia rakoviny iv
Avastin prodlužuje životnost děložního hrdla stádia rakoviny iv Infekční nemoci může způsobit rakovinu
Infekční nemoci může způsobit rakovinu V Americe, vakcína proti rakovině děložního čípku je povinné pro chlapce
V Americe, vakcína proti rakovině děložního čípku je povinné pro chlapce Ve Spojených státech podcenily riziko vzniku rakoviny děložního čípku
Ve Spojených státech podcenily riziko vzniku rakoviny děložního čípku Cervikální příznaky rakoviny, diagnostika a léčba rakoviny děložního čípku
Cervikální příznaky rakoviny, diagnostika a léčba rakoviny děložního čípku Diatermoekstsiziya (electroconization) děložního čípku
Diatermoekstsiziya (electroconization) děložního čípku Provoz Emmett
Provoz Emmett Charakterizace invazivního cervikálního karcinomu
Charakterizace invazivního cervikálního karcinomu Charakteristika předinvazivní rakoviny děložního čípku
Charakteristika předinvazivní rakoviny děložního čípku Charakteristika microinvasive rakoviny děložního čípku
Charakteristika microinvasive rakoviny děložního čípku Léčba prekancerózních procesů
Léčba prekancerózních procesů Léčba pacientů s rakovinou děložního čípku, v kombinaci s těhotenstvím
Léčba pacientů s rakovinou děložního čípku, v kombinaci s těhotenstvím Postnatální vřed dochází 3-4 dny po porodu v důsledku infekce povrchu rány hráze, vaginy a…
Postnatální vřed dochází 3-4 dny po porodu v důsledku infekce povrchu rány hráze, vaginy a… Rekutan (recutanum). Vody a alkoholu, extrakt z heřmánku. Kapalina tmavě hnědé barvy s vůní…
Rekutan (recutanum). Vody a alkoholu, extrakt z heřmánku. Kapalina tmavě hnědé barvy s vůní… Výtahy z gynekologie a porodnictví
Výtahy z gynekologie a porodnictví Souhrny onkologie
Souhrny onkologie Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie.
Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie. Onkologiya-
Onkologiya- Nádory zhps
Nádory zhps