Rakovina genetika

Cancer Genetics.
Video: Diagnostika a genetické aspekty rakoviny prsu. Léčba v Německu
- Buněčný cyklus a jeho regulace.
- Onkogeny a tumor supresorové geny, růst.
Buněčný cyklus a jeho regulace
Všechny zhoubné nádory rozvíjet v důsledku mutací v genech, které regulují buněčný růst. Dělení rakovinných buněk mnoho, jako je rozdělení v normálních buňkách, ale rakovinných buněk často dochází ke ztrátě mechanismy regulace buněčného cyklu.
Buněčný cyklus obvykle skládá ze dvou fází.
- replikace DNA pro S fázi dochází trvání S-fáze, přibližně 8 hodin.
- M-fáze (mitóza) pomocí dělící buňky tvoří dvě dochernie- dobu trvání této fáze - asi 1 hodinu.
Tyto dvě fáze jsou odděleny dvěma dalšími fázemi, při kterých není žádná syntéza DNA nebo dělení buněk.
- G1: mezi N- a S-fazoy- proměnnou dobu trvání.
- G2: mezi S- a M-fáze.
Video: Jak vyléčit rakovinu 4. stupně?
Buňky mohou přejít do klidového stavu a nerozdělují, při výstupu z buněčného cyklu ve fázi G1 a postupuje ve fázi GO.
Mnohé z těchto molekul podílejících se na realizaci buněčného cyklu a její regulace, které byly nainstalovány. Jedna taková skupina z proteinových molekul, které hrají důležitou roli - cyklinů. Indukují buňku rozdělit aktivací cyklin-dependentních kináz (Kč).
Regulace buněčného cyklu
Díky regulaci buněčného cyklu v normální přesně řídit zdvojení DNA a dělení buněk a brání ztrátě genetické informace. Buněčný cyklus má řadu kontrolních bodů, které hrají důležitou roli při ochraně před poškozením normální genomu.
regulaci buněčného cyklu, je nezbytné zachovat integritu normálního genu.
G1-S přechodu
Přechod z G1 fáze do S-fáze, je pod přísnou kontrolou vykonává při zohlednění faktorů jako je velikost buněk, jeho metabolické aktivity, dostupnost růstových faktorů a integrity DNA. Nejdůležitější kontrolní bod v buněčném cyklu - restrikční místa, to bezprostředně předchází vstupu do S-fáze. Průchod skrz tento bod regulována řadou růstových faktorů a důležitých genů, včetně p53.
- Gen p53 hraje klíčovou roli v udržování stability genomu. Rozdělení normálních buněk s poškozenou DNA se zastaví v G1 fázi a p53 gen pod kontrolou chod mechanismu programované buněčné smrti (apoptóze). Tento gen u pacientů s karcinomem nejčastěji podrobí mutací a není překvapující, protože ztráty kontroly nad stability genomu - hlavní rys rakoviny.
- Gen p53 reguluje přechod z fáze M1 do S-fáze.
- Gen p53 považován za „strážce“ genomu.
- P53 nejčastěji mutovaný gen rakoviny.
Buněčný cyklus u rakoviny
Rakovinné buňky jsou charakterizovány porušení buněčného cyklu a jeho regulaci.
Jejich hlavními rysy jsou:
- nekontrolované proliferace, nesplňuje fyziologické potřeby;
- obvyklá délka S- a M-fáze;
- krátké G1-fáze;
- neschopnost kontrolovat body přerušení buněčného cyklu;
- neschopnost spuštění programované buněčné smrti, když je DNA poškozené;
- genomová nestabilita a hromadění více genetických mutací.
Onkogeny jsou geny a nádorový supresor
druhy genů
Ve většině případů, rakovinné buňky jsou monoklonální a jsou odvozeny z jediné buňky, který se nashromáždil několik genových mutací, což vede k nekontrolované proliferaci buněk. V důsledku genetické mutace ke ztrátě funkce genu (inaktivován gen) nebo aktivní (aktivace genu).
Geny nádorový supresor. Funkce těchto genů v karcinogenezi ztracena. Aby se tak stalo, je třeba inaktivace obou kopií genu, tj, supresorový gen je recesivní mutace.
onkogeny. U rakoviny, je funkce těchto genů jsou zesíleny. Proto-onkogeny - non-mutované formy těchto genů v normálním hrají důležitou roli v regulaci buněčné proliferace. Kódují růstové molekuly faktory a jejich receptory, signální molekuly a transkripční faktory. Mutace v onkogenů jsou dominantní.
mutace DNA
DNA Mutace jsou náhodné a v savčích buňkách se vyskytují často (například v důsledku ozáření nebo karcinogenních látek, metabolické poruchy). Díky účinné opravy mechanismy obvykle pouze jeden z 1000 změn bází DNA, což způsobuje mutace.
Následující typy mutací:
- bod (nahrazení jednoho páru bází v molekule DNA do druhého);
- translokace (přeskupování genů v důsledku prasknutí molekuly DNA a jeho opětovné připojení);
- Amplifikace genu (vytvoření více kopií genu);
- delece (ztráta genetického materiálu - z jedné báze do celého genu)
epigenetické změny
Geny supresor nádorového růstu může být inaktivován v důsledku porušení genové exprese bez jakékoli změny nukleotidové sekvence v molekule DNA. Jeden příklad takového mechanismu je methylace promotoru sekvence genu.
Více stupňů transformace nádorové
rakovina - vícestupňový proces vyznačuje akumulací genetických poruch. Zvláště dobře prostudován stadia rakoviny tlustého střeva. Jediná mutace může způsobit benigní buněčné proliferace (přední, například ke vzniku polypů nebo adenomů), predispozicí k vývoji zhoubných nádorů. Mutace v genů zodpovědných za opravy DNA a urychlení procesu.
 Mitosis a meiózy. aneuploidie
Mitosis a meiózy. aneuploidie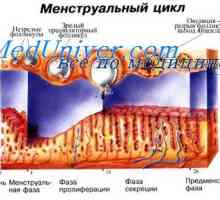 Nádory nadledvinek. Iatrogenní androgenní nadbytek.
Nádory nadledvinek. Iatrogenní androgenní nadbytek. Chemoterapii nádorů. účinky chemoterapie.
Chemoterapii nádorů. účinky chemoterapie.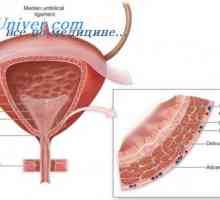 Proliferace fáze menstruačního cyklu. Fáze sekrece děložního cyklu
Proliferace fáze menstruačního cyklu. Fáze sekrece děložního cyklu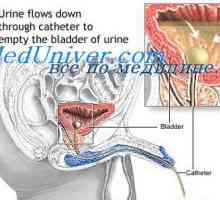 Změny v děloze a vaječníků ve fázi sekrece. Deskvamace fázi regenerace cyklus matka
Změny v děloze a vaječníků ve fázi sekrece. Deskvamace fázi regenerace cyklus matka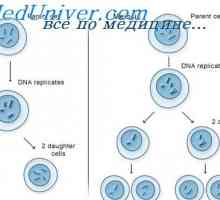 Fáze meiózy a vývoj zárodečných buněk. První meiotické dělení
Fáze meiózy a vývoj zárodečných buněk. První meiotické dělení Ovariální cyklus. Folikulární fáze menstruačního cyklu
Ovariální cyklus. Folikulární fáze menstruačního cyklu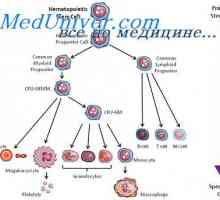 Ovládání diferenciaci kmenových buněk. Zrychlení proliferace kmenových buněk
Ovládání diferenciaci kmenových buněk. Zrychlení proliferace kmenových buněk Enzymatické regulace buněčných funkcí. buněčné dělení
Enzymatické regulace buněčných funkcí. buněčné dělení Regulace buněčného dělení. Diferenciace buněk v tkáni
Regulace buněčného dělení. Diferenciace buněk v tkáni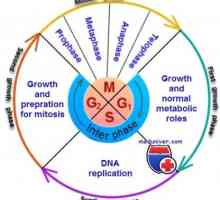 Chromozomu. Mitosis a krok
Chromozomu. Mitosis a krok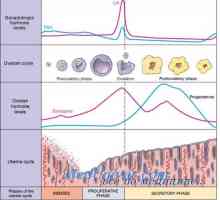 Luteální fáze menstruačního cyklu. předpis
Luteální fáze menstruačního cyklu. předpis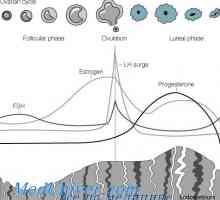 Regulace menstruačního cyklu. Hormony folikulární fáze
Regulace menstruačního cyklu. Hormony folikulární fáze Extrakt z hroznových jader je účinný u kolorektálního karcinomu
Extrakt z hroznových jader je účinný u kolorektálního karcinomu Vědci z nádorových buněk, Mayo Clinic přeprogramovány
Vědci z nádorových buněk, Mayo Clinic přeprogramovány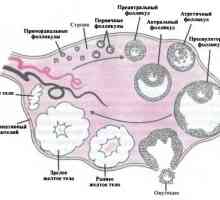 Anatomie a fyziologie ženského reprodukčního referenčního systému
Anatomie a fyziologie ženského reprodukčního referenčního systému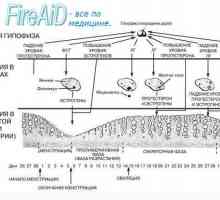 Menstruační cyklus (cyklus matečný louh). Fáze menstruačního cyklu. Menstruační fáze.…
Menstruační cyklus (cyklus matečný louh). Fáze menstruačního cyklu. Menstruační fáze.…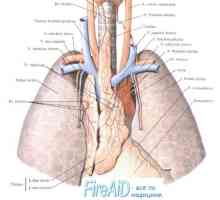 Vzrušivost srdečního svalu. Infarkt akční potenciál. Kontraktility myokardu.
Vzrušivost srdečního svalu. Infarkt akční potenciál. Kontraktility myokardu. Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie.
Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie. Kniha „klinické farmakologie a farmakoterapie“ - hlava 16 léků používaných v…
Kniha „klinické farmakologie a farmakoterapie“ - hlava 16 léků používaných v… Porodnictví a ginekologiya-
Porodnictví a ginekologiya-