Vimizim schválen k léčbě syndromu Morquio
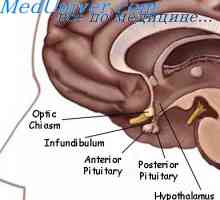
Podání US Food and Drug Administration v pondělí schválila inovativní léčiva Vimizim pro léčbu vzácných onemocnění vrozených enzymových u dětí.Účinná látka je v poloze alfa-Vimizim elosulfaza (elosulfase alfa), která prokázala účinnost v mukopolysacharidózy typu IVA - Morquio syndrom A.
Jedná se o vzácné lysozomální onemocnění s autosomálně recesivní dědičnosti mechanismus, který se vyznačuje nedostatkem acetylgalaktosamin-6-sulfát sulfatázy (GALNS).
Vimizim lék určen k nahrazení chybějících enzymů GALNS, který se podílí na mnoha velmi důležitých metabolických procesů v těle. Deficit tohoto enzymu vede k narušení vývoje kostí, růstové problémy a mobility dítěte.
Ve Spojených státech dnes existuje asi 800 pacientů s Morquio syndromem A.
Droga je FDA Vimizim bylo považováno za prioritní, jako první v historii léku pro léčbu vzácných onemocnění. Tento zjednodušený postup je stanoven předem pouze v případech, kdy je nový lék se očekává zásadní průlom v léčbě některých chorob.
Vimizim také se stal prvním v droze USA získané v rámci přezkumu poukazu nový program s názvem prioritní (Rare Pediatric Priority Disease Review poukaz). Tento program by měl pomoci americkým výzkumným pracovníkům v oblasti vývoje a implementace do klinické praxe nových léků a vakcín, ve kterých pediatrie v krajní nouzi.
„To je rozhodnutí přijato na základě priorit, odráží snahu agentury pro pomoc lidem se vzácným onemocněním. Až do nedávné doby, pacienti s touto vzácnou genetickou poruchou neměl jediného schváleného léčebné možnosti, „- řekl Dr. Andrew Malberg (Andrew Mulberg), výkonný ředitel oddělení gastroenterologie produktů a léčbu vrozených nemocí Centra pro hodnocení a výzkum léčiv (CDER) FDA.
Nejčastějšími nežádoucími účinky u pacientů léčených nového léku, byly: horečka, zvracení, bolest hlavy, bolest břicha, zimnice a únava.
Bezpečnost a účinnost léku Vimizim testována pouze u pacientů starších než 5 let.
Vimizim byl schválen s povinným zahrnutím prevence návodu rizika anafylaktického šoku. V průběhu klinických studií, život ohrožující anafylaktické reakce po podání Vimizim byly zaznamenány u několika pacientů.
Droga je prodávána Vimizim California biofarmaceutická společnost BioMarin Pharmaceutical Inc.
Sdílet na sociálních sítích:
Podobné
 Dehet syndromu u plodu. Aase syndrom, Holt-Oram plod
Dehet syndromu u plodu. Aase syndrom, Holt-Oram plod Klasifikace mukopolysacharidózy. Hurler nemoc, gentera, Sanfilippo, Morquio
Klasifikace mukopolysacharidózy. Hurler nemoc, gentera, Sanfilippo, Morquio FDA schválen dulaglyutid k léčbě diabetu 2. typu
FDA schválen dulaglyutid k léčbě diabetu 2. typu Droga invokana proti diabetu 2. typu, byl schválen FDA
Droga invokana proti diabetu 2. typu, byl schválen FDA FDA schválil olaparib pro léčbu rakoviny vaječníků
FDA schválil olaparib pro léčbu rakoviny vaječníků FDA schválila nový lék pro léčbu rakoviny kůže
FDA schválila nový lék pro léčbu rakoviny kůže Nový lék pro léčbu rakoviny plic gilotrif (afatinib) schválené FDA
Nový lék pro léčbu rakoviny plic gilotrif (afatinib) schválené FDA Nový lék pro léčbu rakoviny močového
Nový lék pro léčbu rakoviny močového V Evropě schválila nový lék pro léčbu rakoviny štítné žlázy lenvima
V Evropě schválila nový lék pro léčbu rakoviny štítné žlázy lenvima Dlouhodobá rizika inhibitory 5-alfa-reduktázy
Dlouhodobá rizika inhibitory 5-alfa-reduktázy Eluksadolin schválen k léčbě syndromu dráždivého tračníku ve Spojených státech
Eluksadolin schválen k léčbě syndromu dráždivého tračníku ve Spojených státech FDA schválila nový lék pro léčbu hemofilie A.
FDA schválila nový lék pro léčbu hemofilie A. FDA schválil tasimelteon k léčbě vzácné poruchy spánku
FDA schválil tasimelteon k léčbě vzácné poruchy spánku Cresemba nový lék pro léčbu plísňových infekcí
Cresemba nový lék pro léčbu plísňových infekcí Uptravi - nový lék proti plicní hypertenzí
Uptravi - nový lék proti plicní hypertenzí Alfa-1-antitrypsin nedostatek, alfa (a) s nízkou molekulovou hmotností antitrypsin inhibitorem…
Alfa-1-antitrypsin nedostatek, alfa (a) s nízkou molekulovou hmotností antitrypsin inhibitorem… FDA schválila nový defibrilátorem eluna
FDA schválila nový defibrilátorem eluna Stiolto Respimat inhalátor k léčbě CHOPN schválený v USA
Stiolto Respimat inhalátor k léčbě CHOPN schválený v USA Ve Spojených státech schválila nový systém pro ERCP Spyglass ds
Ve Spojených státech schválila nový systém pro ERCP Spyglass ds Farmakologické novinky ve Spojených státech a Evropě v září 2013
Farmakologické novinky ve Spojených státech a Evropě v září 2013 Monogenní syndromy mvpr
Monogenní syndromy mvpr