XST jinarc doporučuje lék pro léčbu vzácných onemocnění ledvin
Evropská léková agentura (EMA) doporučuje přípravu přijetí Jinarc (Tolvaptan) pro léčbu autozomálně dominantní polycystické choroby ledvin (ADPKB).Lék zpomaluje Jinarc cystickou degeneraci a pokles funkce ledvin v ADPKB.
Jinarc být používán u pacientů se středně sníženou renální funkce a rychlé progresi onemocnění.
ADPKB v Evropě je velmi vzácné onemocnění, které postihuje 4 osob na 10 tisíc lidí. To je dědičné onemocnění, které je charakterizováno tím, že zvyšuje cysty naplněné tekutinou v ledvinových tkáních. Mezi příznaky patří bolest břicha, problémy s močovým ústrojím, vysoký krevní tlak, časté infekce.
Až do teď, že EU nebyla drogy, speciálně navrženy pro léčbu autozomálně dominantní polycystické choroby ledvin. Současná léčba si klade za cíl odstranit příznaky a prevence komplikací. Je zřejmé, že existuje nenaplněná potřeba účinných léků pro léčbu ADPKB.
Tolvaptan, antagonista vasopresinu V2 receptoru, je již schválen v EU pro léčbu hyponatrémie, ačkoli dávky potřebné k léčbě ADPKB liší. Tolvaptan blokuje ledvinové receptorů, které interagují s vasopresin - regulátor hladiny vody a sodíku v těle.
Předpokládá se, že při ADPKB ledvinové buňky nemohou správně reagovat na vasopresinu, které vede k tvorbě cyst. Příprava Jinarc «deaktivuje“ vasopresinu receptory, a tím zpomaluje progresi onemocnění.
Kladné rozhodnutí Výboru pro léčivé přípravky (CHMP) bylo provedeno na základě výsledků klinického hodnocení, která zahrnovala 1445 dospělých s ADPKB. Příjem Jinarc léčivo vedlo k významnému zpomalení progrese onemocnění ve srovnání s placebem. Pozorování trvalo tři roky.
Výbor doporučuje další monitorování rizika onemocnění jater v léčbě drogové Jinarc, protože během testování závažné vedlejší účinky v játrech bylo hlášeno u 2,3% pacientů na Jinarc oproti 1,0% pacientů užívajících placebo. Ačkoli případy selhání jater nebyla tato možnost by neměl být zlikvidován při použití ve velkém měřítku léku. EMA varují, že tolvaptan může způsobit poškození jater, což může vést k selhání.
Jinarc pokud slouží k přiřazení další monitorování, včetně krevních testů jaterních testů. Analýzy by měly být provedeny před zahájením léčby a potom každý měsíc po dobu 18 měsíců a poté každé 3 měsíce až do konce příjmu. Lék by měl jmenovat lékaře, který se specializuje na léčbu ADPKB a plně pochopit rizika terapie tolvaptanom.
Nové léčivo EMA byla zkoumána zjednodušeným postupem pro vzácná léčiva pro léčbu vzácných onemocnění. CHMP stanovisko výboru je rozhodující pro schválení Jinarc a jeho zavedení do klinické praxe v EU.
Sdílet na sociálních sítích:
Podobné
 Multicystická ledvin dysplazie plod. Retsissivnaya fetální polycystické onemocnění ledvin
Multicystická ledvin dysplazie plod. Retsissivnaya fetální polycystické onemocnění ledvin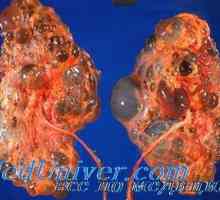 Autozomálně dominantní polycystické onemocnění ledvin u dětí. Diagnostika a léčba
Autozomálně dominantní polycystické onemocnění ledvin u dětí. Diagnostika a léčba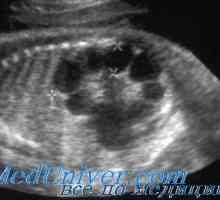 Autosomálně recesivní polycystické onemocnění ledvin u dětí. Diagnostika a léčba
Autosomálně recesivní polycystické onemocnění ledvin u dětí. Diagnostika a léčba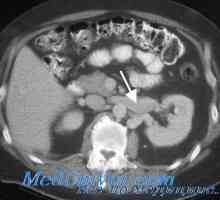 Trombóza ledvinových žil u dětí. Diagnostika a léčba
Trombóza ledvinových žil u dětí. Diagnostika a léčba Chronické selhání ledvin u dětí. důvody
Chronické selhání ledvin u dětí. důvody V Evropě schválila nový lék pro léčbu rakoviny štítné žlázy lenvima
V Evropě schválila nový lék pro léčbu rakoviny štítné žlázy lenvima Diferenciální diagnóza rakoviny ledvin
Diferenciální diagnóza rakoviny ledvin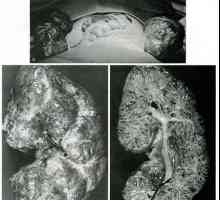 Vývojové stav ledvin abnormality a. Cystická renální anomálie
Vývojové stav ledvin abnormality a. Cystická renální anomálie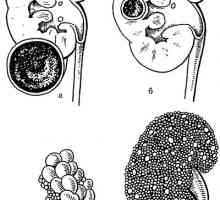 Diagnóza retroperitoneální nádorů. Výskyt vrozených cyst
Diagnóza retroperitoneální nádorů. Výskyt vrozených cyst Použití inhibitorů ACE pro CRF kroku
Použití inhibitorů ACE pro CRF kroku Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie.
Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie. Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie.
Zdraví encyklopedie, nemoc, léky, lékař, lékárna, infekce, souhrny, sex, gynekologie, urologie. Terapie, polycystické ledviny
Terapie, polycystické ledviny Léčba onemocnění ledvin,
Léčba onemocnění ledvin, Léčba onemocnění ledvin,
Léčba onemocnění ledvin, Terapie
Terapie Chronické onemocnění ledvin a hypertenze
Chronické onemocnění ledvin a hypertenze Autozomálně dominantní polycystické onemocnění ledvin
Autozomálně dominantní polycystické onemocnění ledvin Dědičná nefropatie
Dědičná nefropatie Multicystická onemocnění ledvin
Multicystická onemocnění ledvin Jiné patologie novorozenců
Jiné patologie novorozenců